Прививка по экстренной схеме

21 2021. N1//1-333 ” — COVID-19 “
” — COVID-19 “, COVID-19 ( ” ” ) “”.
: 33 . 1 .
” — COVID-19 “
COVID-19 ( ” ” ) , “”.
1.
1.1. COVID-19 .
1.2. , , COVID-19 , COVID-19 .
1.3. , – , ” ( )” .
2. COVID-19
2.1. COVID-19 – , , , , () ” ( )”.
2.2. COVID-19 , , .
2.3. COVID-19 . , – , . , () ” ( )”.
2.4. COVID-19 . COVID-19 , , , , , ” “.
2.5. .
2.6. , , , ( ), , ” ” , .
2.7. COVID-19 “–” ( – ), , , , .
2.8. .
2.9. : (COVID-19) 18 .
2.10. :
– – , ;
– ;
– , – 2-4 . , ;
– ;
– 18 ( ).
2.11. II:
( , , , 40 ..) I .
2.12. : , ( ), , , , , , .
2.13. :
– ( , , );
– .
2.14. : , , . , , , , 1 – .
2.15. .
3.
3.1. , .
4.
4.1. – .
4.2. :
– (, );
– (, , );
– ;
– COVID-19.
5. COVID-19
5.1. COVID-19 , , , . .
5.2. COVID-19 , , , , , ( N1), ( N4), 20 21.11.2011 N323- ” “.
5.3. (, -) , , ( ), , , , – , COVID-19 ( N3). ( N2).
5.4. , (, -) .
5.5. COVID-19 , , .
5.6. ( 18) , , , , .
5.7. I II . 3,0 . 0,5 . : , !
5.8. . .
5.9. ( ), – ). .
5.10. ().
5.11. “–” , . I II COVID-19 .
6. COVID-19
6.1. , , , , , COVID-19 *.
6.2. COVID-19 ( ):
7. COVID-19
7.1. , , , , , COVID-19 .
7.2. COVID-19 ( ):
7.3. , , .
7.4. , .
7.5. , , , .
7.6. COVID-19 (-, , -).
7.7. :
– COVID-19 ;
– , ;
– , ;
– , , , ( ) ;
– ;
– , , ;
– , – ;
– .
8.
8.1. – (0,5 / ) (3,0 ). , 3,0 , , 5 0,5 . 3,0 2 . 0,5 . 0,5 .
8.2. I II . : , , !
8.3. , . . , . . 2,0 , 0,5 , . ( ) .
8.4. . . ( ). – .
8.5. : I 0,5 , 21 II 0,5 .
9.
9.1. 15.02.2017 N1071 ” ” .
9.2. ” , ” ( 12.04.2019).
9.3. () (, -) : (. 025-87), (. 156/-93), (. 064).
9.4. , , (. 060), – (.110/) (. 003-1/).
9.5. (), , , () :
– , , ;
– () (), , .
9.6. () (), , , , , :
– 2 ( , , , , ), , – ; () ;
– ;
– 12 – ( ) (), , :
– () , – ( 04.02.2016 N11 ” – “;
– “” ( ).
9.7. , , , .
9.8. , , , , :
– ,
– /
– /
– , , , , .
– ()
– –
– /
– , , , , , ,
– , ,
9.9. () ( ), , (, , , , .), , , () ().
9.10. ( – ), ().
9.11. ( 1 ” , “, 12.04.2019)), ( 6 ).
9.12. – (, , -, ) .
9.13. () , , ( ) # ( ” 2.0″ ), .
9.14. , 12.04.2010 N61- ” “.
10. , “–“
10.1. “–” , , .
10.2. , , .
10.3. , , .
10.4. , “–“, .
10.5. “–” – , . .
10.6. , “–” .
10.7. .
10.8. “–” , . .
10.9. :
– ( );
– ( );
– -, ( ).
10.10. , “–” .
10.11. , “–” , , , , , – , 4.
10.12. .
10.13. – , , .
10.14. , (, ), , .
10.15. “–” , , .
10.16. ” ” “–” .
10.17. “–” , , , . , () “–“, ( 18 ) .
10.18. “–” , ” ” , , ” ” . 3.3.2.3332-16.
10.19. ( ).
11. /
11.1. – , .
11.2. / , ().
11.3. / , , .
11.4. / , , .
11.5. . . . , , , , .
11.6. . .
11.7. :
– , ;
– ;
– ;
– ;
– / ;
– ;
– .
11.8. / () .
11.9. , /, .
11.10. / : ( ), , /. , . , , .
11.11. . / , . , , .
12.
– 17.07.1998 N157- ” “;
– 21.11.2011 N323- ” “;
– 12.04.2010 N61- ” “;
– 16.04.2012 N291 ” ( , , , “”)”;
– 15.05.2012 N543 ” – “;
– 31 2020. N373 ” (COVID-19)”;
– 03.03.2008 N15 ” – 3.3.2342-08″ ( ” 3.3.2342-08. . – “);
– 04.06.2008 N34 ” – 3.3.2367-08″ ( ” 3.3.2367-08. . – “);
– 3 2020. N41 ” – 3.1.3671-20 ” (COVID-19) –“;
– 03.04.2020 N440 ” 2020 “;
– 16.04.2012 N291 ” ( , , , “”)”;#
– / ;
– ” , “, 12.04.2019;
– 15.02.2017 N1071 ” “.
13. , ,
______________________________
* ( 1) COVID-19 ( 2):
– 1 , 1 – 60 ;
– 2 , 1 – 120 ;
– 3 , 1 – 180 . ( : 10 ./ – , 30 ./ – , ()).
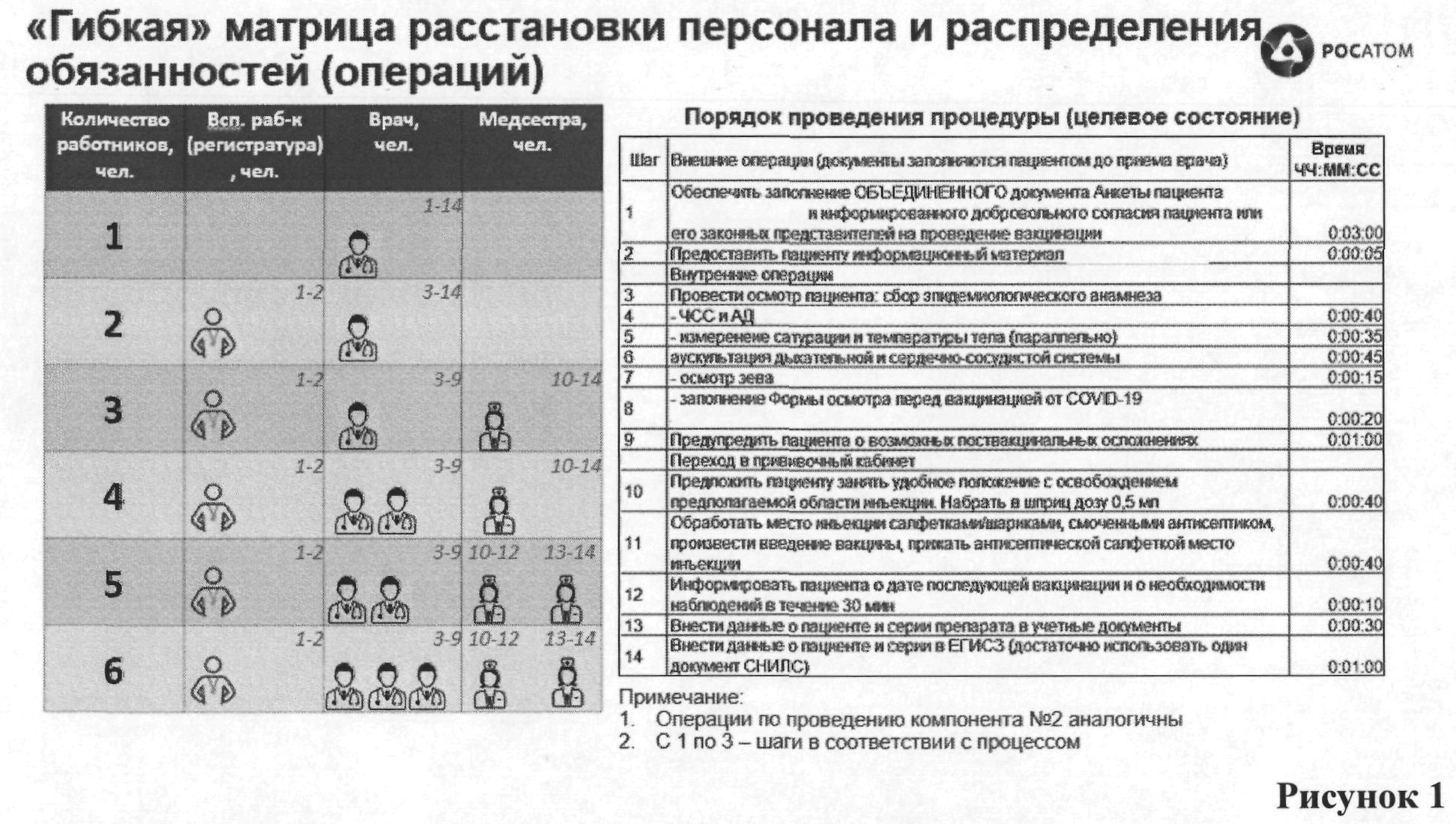

N1
N2
“–” – , SARS-CoV-2
:
I (, , ) ________________________________
II (, , ) ________________________________
:
– ( , , , , , , , ) ( , , ) . , , , – . .
3- , , , , . , , . – .
3 . – .
N3
COVID-19
:
COVID-19 ()
____________________________ ___________________________
N4
COVID-19 “–“
!
– ! , , ( ) , :
1. , COVID-19 G SARS-CoV-2 .
2. :
– – , ;
– ;
– ;
– ( 2-4 );
– ;
– 18 .
3. , , , – .
.
4. : I 0,5 . . 21 II 0,5 . .
5. 30 .
6. ( I II ) – ( , , , , , , , ) ( , , ) .
, , , – . .
3- , , , , .
, , . – .
COVID-19 , .
COVID-19 –. . , . .
Источник
Началась вакцинация препаратом “Ковивак”, разработанным Центром им. М.П. Чумакова. Это третья вакцина, одобренная для применения в России, – после “Спутника V” от Центра эпидемиологии и микробиологии имени академика Гамалеи и “Эпиваккороны” от Центра “Вектор”. Четвертой зарегистрированной в стране вакциной стал “Спутник Лайт”, поступить в гражданский оборот он может уже в июне.
Все вакцины получили регистрацию в экстренном порядке, до окончания третьей фазы клинических исследований, – в связи с положительными результатами первых двух. Сейчас только вакцина “Спутник V” прошла все четыре стадии исследований: одну доклиническую (на животных) и три клинических (на людях). “Эпиваккорона” уже проходит третью фазу, а разработчики “Ковивака” набирают добровольцев для ее начала. Кроме того, 19 февраля начались международные клинические испытания препарата “Спутник Лайт”, разработанного на базе вакцины от Центра им. Гамалеи. В них участвуют в общей сложности 6 тыс. добровольцев.
Чем отличаются и как работают вакцины
“Спутник V” – комбинированная векторная вакцина. Она состоит из двух доз, в составе которых находятся неспособные к размножению аденовирусы-векторы, которые доставляют в организм ген коронавирусного S-белка. После прививки клетки организма начинают производить этот белок, а иммунная система реагирует на него. Антитела к этому белку (точнее, к его рецептор-связывающему домену) считаются нейтрализующими, то есть препятствующими заражению.
“Эпиваккорона” – пептидная вакцина. В отличие от “Спутника V” она не несет в себе биологического агента и состоит из искусственно синтезированных коротких фрагментов вирусных белков (пептидов), через которые иммунная система обучается и в дальнейшем распознает и нейтрализует вирус.
“Ковивак” – это так называемая цельновирионная вакцина. В ее основе используется коронавирус SARS-CoV-2, который специально обработан так, что лишился своих инфекционных свойств, но при этом сохраняет способность вызывать иммунную реакцию. Она формирует комплексный иммунный ответ на все белки коронавируса, а не только на S-белок или его компоненты.
“Спутник Лайт” – это векторный препарат на основе аденовируса человека, который используется для транспортировки генетической информации коронавируса SARS-CoV-2. Вакцина является первым компонентом “Спутника V” и не требует введения второй дозы.
У “Спутника V” и “Эпиваккороны” интервал между инъекциями составляет три недели, а у “Ковивака” – две недели.
Эффективность и безопасность вакцин
Вакцина “Эпиваккорона” успешно прошла первую и вторую фазы клинических испытаний, а “Спутник V” – все три фазы. Публикации с результатами финальных испытаний “Спутника V” вышли в авторитетном научном журнале The Lancet. Результаты первой-второй фаз испытаний “Эпиваккороны” опубликованы в российском научном журнале “Инфекция и иммунитет”.
Эффективность вакцины “Спутник V” составила 91,6%. Среди добровольцев старше 60 лет она оказалась еще выше – 91,8%. Антитела к коронавирусу после вакцинации российским препаратом были обнаружены у 98% добровольцев. Клеточный иммунитет сформировался у всех участников испытаний. Иммунитет после прививки оказался в 1,3-1,5 раза выше, чем после перенесенного заболевания.
У “Спутника V” также один из самых низких рисков серьезных побочных эффектов – 0,27% против 0,58% у вакцины Pfizer – BioNTech и 0,97% у разработки Moderna.
Аллергических реакций и анафилактического шока после вакцинации “Спутником V” зафиксировано не было.
Разработчики “Спутника V” утверждают, что после вакцинации двумя дозами препарата люди перестают быть разносчиками коронавируса. Но вопрос о ношении ими масок еще не решен.
О стопроцентной иммунологической эффективности “Эпиваккороны” в январе сообщила пресс-служба Роспотребнадзора. Оценки эффективности “Эпиваккороны” по данным исследований пока не опубликованы.
Разработчики вакцины “Ковивак” не раскрывали подробные данные о ее эффективности. По словам директора центра Айдара Ишмухаметова, эффективность в течение двух недель после введения второй инъекции вакцины составляет 70%, а к 21-му дню повышается до 90%. Статью об эффективности вакцины, как сообщает разработчик, стоит ждать в августе-сентябре.
Людям в возрасте 60 и более лет, вероятно, понадобится на одну дозу больше вакцины от коронавируса “Ковивак” – три, а не две, так как у них снижен иммунный ответ, сообщил генеральный директор Центра имени М.П. Чумакова. Это станет известно точно после проведения исследования эффективности вакцины для населения в возрасте 60+.
Все вакцины рекомендованы для лиц в возрасте от 18 до 60 лет. Расширение показаний к применению будет возможно после прохождения клинических исследований с участием добровольцев старше 60 лет и добровольцев с сопутствующими заболеваниями.
Продолжительность действия защиты вакцин неизвестна.
Выпуск препаратов
По состоянию на конец апреля в гражданский оборот поступило 16 млн доз “Спутника V”, 1,3 млн доз “Эпиваккороны” и 120 тыс. доз “Ковивака”.
Производство вакцин от коронавируса ориентировано в первую очередь на внутренний рынок.
По данным от 9 апреля, вакцина “Спутник V” также была одобрена к применению в 60 странах. Помимо России это Белоруссия, Аргентина, Боливия, Сербия, Алжир, Палестина, Венесуэла, Парагвай, Туркменистан, Венгрия, ОАЭ, Иран, Республика Гвинея, Тунис, Армения, Мексика, Никарагуа, Республика Сербская (энтитет Боснии и Герцеговины), Пакистан, Монголия и другие.
Вакцинация
Прививочная кампания в России стартовала 5 декабря. Первыми получили возможность записаться на прививку те, у кого риск заражения выше в силу профессиональной деятельности: врачи, соцработники, работники торговли и сферы услуг, промышленности, транспортной сферы, СМИ и спорта.
18 января началась массовая вакцинация – для всех категорий граждан.
По данным, озвученным министром здравоохранения Михаилом Мурашко 27 мая, почти 17 млн россиян провакцинированы первым компонентом. Полностью прошли вакцинацию 10 млн человек, переболели коронавирусной инфекцией почти 4,8 млн.
Вакцинация добровольная и бесплатная для граждан России.
Противопоказания и побочные эффекты
Вакцины противопоказаны людям с гиперчувствительностью к какому-либо из их компонентов, склонностью к тяжелым аллергическим реакциям, беременным и кормящим грудью, а также людям в возрасте до 18 лет. Препарат от Центра “Вектор” противопоказан людям с первичным иммунодефицитом и злокачественными заболеваниями крови. При температуре выше 37°С вакцинацию не проводят. В инструкции к препарату от Центра им. Гамалеи также указано, что прием препаратов, угнетающих функцию иммунной системы, противопоказан как минимум за один месяц до и после вакцинации.
В инструкциях к вакцинам есть предупреждение, что с осторожностью следует вакцинироваться людям с хроническими заболеваниями печени и почек, выраженными нарушениями функции эндокринной системы (сахарным диабетом), тяжелыми заболеваниями системы кроветворения, эпилепсии, а также при инсультах и других заболеваниях центральной нервной системы, заболеваниях сердечно-сосудистой системы, аутоиммунных заболеваниях. В инструкции к вакцине от Центра им. Гамалеи в этом списке также указаны заболевания легких, астма, атопия и экзема.
При тяжелых реакциях на первый компонент вакцин второй вводить запрещается.
Побочными действиями вакцины от Центра “Вектор” указаны боль в месте введения и (часто) кратковременное повышение температуры не выше 38,5°С. В инструкции к препарату от Центра им. Гамалеи указаны такие возможные реакции, как гриппоподобный синдром (с ознобом, повышением температуры тела, артралгией, миалгией, астенией, общим недомоганием, головной болью), реже – тошнота, диспепсия, снижение аппетита, иногда – увеличение регионарных лимфоузлов.
После введения вакцины пациент должен находиться под наблюдением медицинских работников в течение 30 минут.
Вакцинация “Ковиваком” противопоказана при беременности и во время грудного вскармливания, так как эффективность и безопасность препарата в этот период не изучались. Выводы о возможности применения “Спутника V” беременным сделают в июне-июле.
К другим противопоказаниям применения “Ковивака” относятся тяжелые аллергические реакции, серьезные реакции после введения препарата на любую предыдущую вакцинацию в анамнезе (температура выше 40 градусов, гиперемия или отек более 8 см в диаметре) или таких осложнений, как коллапс или шокоподобное состояние, развившихся в течение 48 часов после вакцинации.
Источник
Врачи часто забывают проводить профилактику столбняка пациентам, что служит потом поводом для разбирательств. Правила выполнения профилактики регулируются в России приказом МЗ РФ от 17.05.99 N 174 «О мерах по дальнейшему совершенствованию профилактики столбняка» Приказ достаточно объемный, ниже перечислены только извлечения, которые касаются вопросов экстренной профилактики.
- Экстренная профилактика столбняка
- Иммунологический контроль при экстренной профилактике столбняка
- Назначение препаратов
- Активно-пассивная профилактика столбняка
- Противопоказания
Экстренная профилактика столбняка
Экстренная профилактика столбняка начинается с первичной хирургической обработки раны и одновременной специфической иммунопрофилактики. Экстренную иммунопрофилактику столбняка нужно провести как можно раньше и аж до 20 дня с момента получения травмы, учитывая длительность инкубационного периода при заболевании столбняком.
Экстренную профилактику столбняка проводят при:
- обморожениях и ожогах (химических, термических, радиационных) 2-й, третьей и четвертой степени;
- травмах, при которых было нарушение целостности кожных покровов и слизистых оболочек;
- абортах, сделанных вне больничных учреждений;
- проникающих повреждениях ЖКТ;
- гангрене или некрозе тканей любого типа, длительно текущих карбункулах, абсцессах;
- родах вне медицинских учреждений (например, в домашних условиях);
- укусах животными.
Примечание
<1> Вместо 0,5 мл адсорбированного столбнячного анатоксина можно применять АДС-М, если необходима вакцинация против дифтерии этим средством. Если локализация раны позволяет, АС предпочтительно вводить в область ее расположения путем подкожного обкалывания.
<2> Применять один из указанных препаратов: ПСЧИ или ПСС (предпочтительнее вводить ПСЧИ).
<3> При “инфицированных” ранах вводят 0,5 мл АС, если после последней ревакцинации прошло 5 и более лет.
<4> Полный курс иммунизации АС для взрослых состоит из двух прививок по 0,5 мл каждая с интервалом 30-40 дней и ревакцинации через 6-12 мес. той же дозой. По сокращенной схеме полный курс иммунизации включает однократную вакцинацию АС в удвоенной дозе (1 мл) и ревакцинацию через 1-2 года дозой 0,5 мл АС.
<5> Две прививки по обычной схеме иммунизации (для взрослых и детей) или одна прививка по сокращенной схеме иммунизации для взрослых.
<6> При “инфицированных” ранах вводят ПСЧИ или ПСС.
<7> Все люди, которым сделали активно-пассивную профилактику, для завершения курса иммунизации через 6 мес. – 2 года должны быть еще раз вакцинированы АС в объеме 0,5 мл.
<8> После нормализации посттравматического состояния детей нужно привить АКДС-вакциной.
Препараты для экстренной иммунопрофилактики столбняка
- Адсорбированный дифтерийно-столбнячный анатоксин с уменьшенным содержанием антигенов (АДС-М);
- Адсорбированный столбнячный анатоксин (АС);
- Сыворотка противостолбнячная лошади.
Иммунологический контроль при экстренной профилактике столбняка
При отсутствии достоверных сведений о прививках состояние противостолбнячного иммунитета оценивается непосредственно в момент обращения больного по поводу травмы. Схема выбора экстренной профилактики основывается на результатах определения уровня специфического антитоксина в сыворотке крови пациента с травмой либо – на косвенных критериях факта проведения прививки против столбняка (возраст, пол, отсутствие противопоказаний, служба в армии и пр.)
Достаточный для исследования объем крови 0,2 мл – может быть получен из раны или одновременно со взятием крови из пальца для проведения любого клинического анализа. Забор крови осуществляется в капилляр или пробирку, которую оставляют при комнатной температуре или в бытовом холодильнике на 15-20 минут, после чего надосадочную над эритроцитами жидкость (сыворотку) используют для проведения серологических исследований.
При взятии крови из вены используют стандартный способ отделения сыворотки крови. Определение столбнячного антитоксина в сыворотке крови больного осуществляется в РПГА в соответствии с инструкциями по применению диагностикумов. Минимальный титр столбнячного антитоксина, свидетельствующий о проведенной иммунизации, равен 1:20.
Назначение препаратов
Назначение препаратов для экстренной иммунопрофилактики столбняка проводится дифференцированно в зависимости от наличия документального подтверждения о проведении профилактической прививки или данных иммунологического контроля напряженности противостолбнячного иммунитета, а также с учетом характера травмы.
Введение препаратов не проводится
- детям и подросткам, которые имеют документальное подтверждение о проведении плановых профилактических прививок, которые положены им по возрасту, независимо от времени, которое прошло после очередной прививки;
- взрослым людям, имеющим документальное подтверждение о проведенном полном курсе иммунизации не более пяти лет назад;
- людям, имеющим титр столбнячного антитоксина в сыворотке крови выше 1:160 по данным РПГА (согласно данным экстренного иммунологического контроля), что соответствует титру выше 0,1 МЕ/мл по данным биологической peaкции нейтрализации – РН (защитный титр).
Вводят только 0,5 мл АС-анатоксина
- взрослым людям, имеющим документальное подтверждение о проведенном полном курсе иммунизации более 5 лет назад;
- детям и подросткам, имеющим документальное подтверждение о проведении курca плановых профилактических прививок без последней возрастной ревакцинации, независимо от срока последней прививки;
- лицам, имеющим, по данным экстренного иммунологического контроля, титр столбнячного анатоксина в пределах 1:20-1:80 по данным РПГА или в пределах 0,01-0,1 МЕ/мл по данным РН;
- лицам всех возрастов, получившим две прививки не более 5 лет назад, либо одну прививку не более 2 лет назад; детям с 5-месячного возраста, подросткам, военнослужащим срочной службы и отслужившим в армии установленный срок, прививочный анамнез которых не известен, а противопоказаний к проведению прививок не было.
Вместо 0,5 мл АС можно вводить 0,5 мл АДС-М, если необходима иммунизация этим препаратом.
Экстренную профилактику столбняка осуществляют с соблюдением следующих правил:
- перед введением ампулу с препаратом тщательно просматривают. Препарат не подлежит применению в следующих случаях:
- – при отсутствии на этикетке полных сведений о препарате;
– при отсутствии на ампуле этикетки;
– при наличии неразбивающихся хлопьев, осадка или посторонних включений (волокна, пригар и др.);
– при наличии трещин на ампуле;
– в случае неправильного хранения препарата;
– в случае истекшего срока годности лекарственного средства;
- непосредственно перед введением АС ампулу встряхивают до получения гомогенной взвеси;
- при вскрытии ампулу до и после надреза напильником протирают стерильной ватой, смоченной спиртом. Вскрытую ампулу с АС или ПСС можно хранить, накрыв стерильной салфеткой, в течение не более 30 минут;
- препараты набирают в шприц из ампулы длинной иглой с широким просветом. Для инъекции используют обязательно другую иглу;
- кожу на месте укола дезинфицируют 70%-ным спиртом;
- после введения препарата место укола смазывают йодом или спиртом.
Экстренная профилактика путем ревакцинации
АС вводят в количестве 0,5 мл в соответствии с инструкцией к препарату. Если позволяет локализация раны, предпочтительно вводить АС-анатоксин в регион ее расположения путем подкожного обкалывания.
Активно-пассивная профилактика столбняка
АС нужно ввести в объеме 1 мл, перед этим ознакомившись с инструкцией к препарату. Вместе с этим в другой участок тела нужно ввести ПСЧИ 250 ME в/м, при отсутствии ПСЧИ вводят 3000 ME ПСС. Перед введением ПСС обязательно ставят внутрикожную пробу с лошадиной сывороткой, разведенной в пропорции 1:100, для определения чувствительности к белкам сыворотки лошади (ампула маркирована красным цветом). Внутрикожную пробу нельзя ставить, если пострадавшему на протяжении 1-3 суток перед введением ПСС проба была проведена с разведенным 1:100 антирабическим гаммаглобулином из сыворотки лошади в связи с необходимостью введения антирабического гаммаглобулина.
Для постановки пробы нужно применить индивидуальную ампулу, а также стерильные шприцы с делениями на 0,1 мл и тонкую иглу. Разведенную 1:100 сыворотку вводят под кожу в сгибательную поверхность предплечья в колиестве 0,1 мл. Реакцию контролируют спусатя 20 минут. Пробу считают отрицательной, если диаметр отека или покраснения на месте введения менее 1,0 сантиметра.
Проба считается положительной, если отек или покраснение в диаметре равняются 1,0 см и более. При отрицательной кожной пробе ПСС (из ампулы, маркированной синим цветом) вводят подкожно в объеме 0,1 мл. При отсутствии реакции спустя пол часа, нужно ввести стерильным шприцем остальную дозу сыворотки. На протяжении этого срока вскрытая ампула с ПСС должна быть закрыта стерильной салфеткой.
Примечание. Людям с аллергическими болезнями и реакциями на различные аллергены, а также получавшим ранее препараты, содержащие лошадиную сыворотку (ПСС и другие) или гетерологичные гаммаглобулины (антирабический, противоэнцефалитный и др.), перед введением основной дозы ПСС лучше всего прибегнуть к введению антигистаминных лекарственных средств.
Лицам с положительной реакцией на внутрикожное введение 0,1 мл разведенной 1:100 лошадиной сыворотки или имевшим реакцию на подкожное введение 0,1 мл ПСС, дальнейшее введение ПСС проводить нельзя.
Учитывая, что после введения ПСС и препаратов, в составе которых есть столбнячный анатоксин, у особо чувствительных лиц может развиться шок, за каждым привитым необходимо организовать медицинское наблюдение на протяжении 60 минут после прививания. А учреждение, в котором людям делают прививки, должно быть обеспечено средствами противошоковой терапии на случай необходимости.
Противопоказания к применению специфическиз средств экстренной профилактики столбняка
Основными противопоказаниями к применению средств специфической профилактики столбняка являются:
- беременность (в первой половине противопоказано введение АС (АДС-М) и ПСС, во второй половине – ПСС);
- повышенная чувствительность к соответствующему средству профилактики;
- у лиц, имевших противопоказания к введению АС (АДС-М) и ПСС, возможность проведения экстренной профилактики с помощью ПСЧИ определяется лечащим врачом.
Состояние алкогольного опьянения не является противопоказанием к экстренной профилактике.
Источник
